中国网2月25日讯 据英国路透社报道,康希诺生物股份公司(以下简称“康希诺生物”)24日发布公告称,其与中国军事医学研究院联合研发的重组新型冠状病毒疫苗(5型腺病毒载体)(Ad5-nCoV)克威莎TM附条件上市申请已获得中国国家药品监督管理局受理。同日,国药集团中国生物武汉生物制品研究所也表示,已正式向国家药监局提交新冠灭活疫苗附条件上市申请,并获得受理。这意味着中国可能即将拥有4款附条件上市的新冠疫苗。
报道称,目前中国已批准2款国产新冠疫苗附条件上市,即国药集团中国生物和北京科兴中维的新冠病毒灭活疫苗。这些中国产疫苗在许多受疫情影响严重的发展中国家大受欢迎。
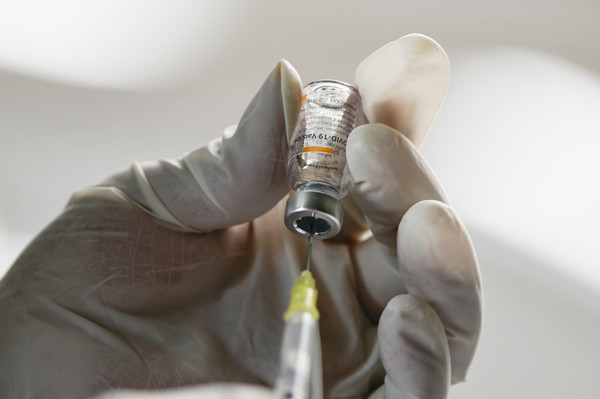
2月22日,在墨西哥埃卡特佩克,医务人员进行新冠疫苗接种的准备工作。新华社记者 辛悦卫 摄
报道援引武汉生物制品研究所表示,该机构已于2020年7月起在阿联酋等多国开展了“新冠灭活疫苗Ⅲ期临床试验”。经统计分析,疫苗接种后安全性良好,疫苗针对由新冠病毒感染引起的疾病(COVID-19)的保护效力为72.51%。
另外,康希诺生物表示,其重组新冠疫苗克威莎TM的Ⅲ期临床试验期中分析数据结果显示,在单针接种疫苗14天后,疫苗对所有症状总体保护效力为68.83%。在疫苗对重症的保护效力方面,单针接种疫苗28天和14天后分别为90.07%和95.47%。该疫苗已在巴基斯坦和墨西哥获得紧急使用授权,并于去年6月获得中国军队特需药品批件,可作为军队应急使用。
根据数据结果,武汉生物制品研究所和康希诺生物的新冠疫苗均达到世界卫生组织相关技术标准及中国国家药品监督管理局印发的《新型冠状病毒预防用疫苗临床评价指导原则(试行)》中的相关标准要求。
据了解,各款中国产疫苗均可在普通冷藏温度下稳定保存,更易于正常运输及存储,疫苗可及性更高,因此也成为广大发展中国家的首选。
中国外交部发言人汪文斌23日表示,中国正在向53个有需求的国家提供疫苗无偿援助,也在向27个愿意购买中国疫苗的国家出口疫苗。












